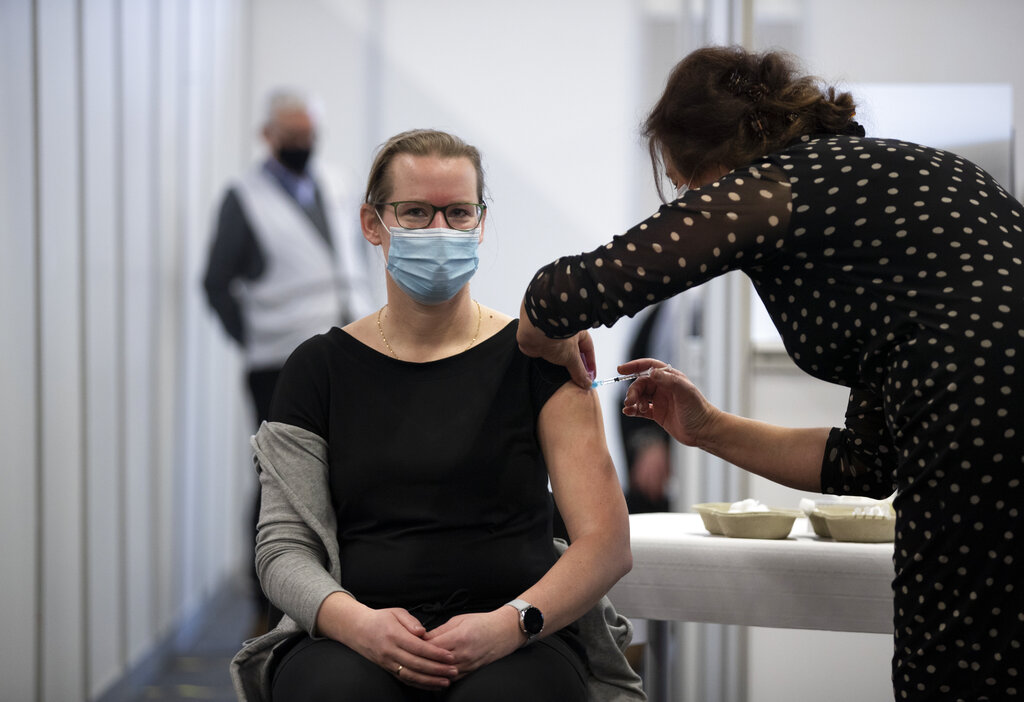
La farmacéutica estadounidense Pfizer y su socia alemana BioNTech, cuya vacuna contra el coronavirus fue la primera en recibir autorización para uso de emergencia en los Estados Unidos, han solicitado que se permita aplicarla a una cantidad más amplia de adolescentes.
Las compañías han solicitado a la Administración de Alimentos y Medicamentos de Estados Unidos (FDA por sus siglas en inglés) que amplíe la autorización al uso de emergencia de su vacuna para incluir a adolescentes de entre los 12 y los 15 años de edad. A mediados de diciembre, se autorizó el uso de emergencia de su vacuna de dos dosis para aplicarla en personas de 16 años y más.
Pfizer y BioNTech dijeron que trabajan estrechamente con la FDA y reguladores de otras naciones para conseguir una autorización condicional de emergencia lo más rápido posible para adolescentes de 12 a 15 años.
Ambas empresas subrayaron en un comunicado que los resultados preliminares llevados a cabo hasta el pasado 31 de marzo de los ensayos clínicos en ese grupo etario muestran que la vacuna es segura y 100% efectiva para impedir infecciones. Dijeron que los efectos colaterales coincidieron con los de las pruebas con voluntarios de 16 a 25 años: dolor e inflamación en el lugar de la inyección, fatiga, dolor de cabeza, fiebre y náusea. /JU
Foto: AP News